Journal of Hepatology (IF=25.7)在线发表题为“Increased Siglec-9/Siglec-9L interaction in NK cells predicts poor HCC prognosis and can be a targetable checkpoint for immunotherapy”的研究论文。山东大学基础医学院教授马春红、梁晓红,药学院教授刘新泳以及山东大学齐鲁医院病理科教授韩博作为共同通讯作者,博士研究生肖榕、博士后田野为共同第一作者,山东大学为第一作者单位和唯一通讯作者单位。
肝细胞肝癌(HCC)发病率高、死亡率高,是全球第三大癌症相关死亡原因。近年来,免疫检查点抑制剂(ICIs)为肝癌的治疗带来了革命性的突破,但总体缓解率较低且易在全身多器官导致免疫相关不良反应,因此,有必要进一步探索寻找更好地治疗肝癌的免疫检查点靶点及药物。NK细胞具有强大的杀伤肿瘤细胞的能力,在肝脏中含量丰富,其表面活化性和抑制性受体有平衡控制NK细胞的功能。异常唾液酸化是肝癌等多种肿瘤的特性,唾液酸化蛋白可以作为NK细胞抑制性受体的配体,限制NK细胞的免疫监视作用。Siglecs作为唾液酸化蛋白的受体家族蛋白,近年作为新兴的免疫检查点受到了广泛的关注,其中Siglec-7和Siglec-9是主要表达在人NK细胞上的两个Siglec家族蛋白,但其在HCC微环境中的空间互作网络及其作为治疗靶点的潜力尚不明确。
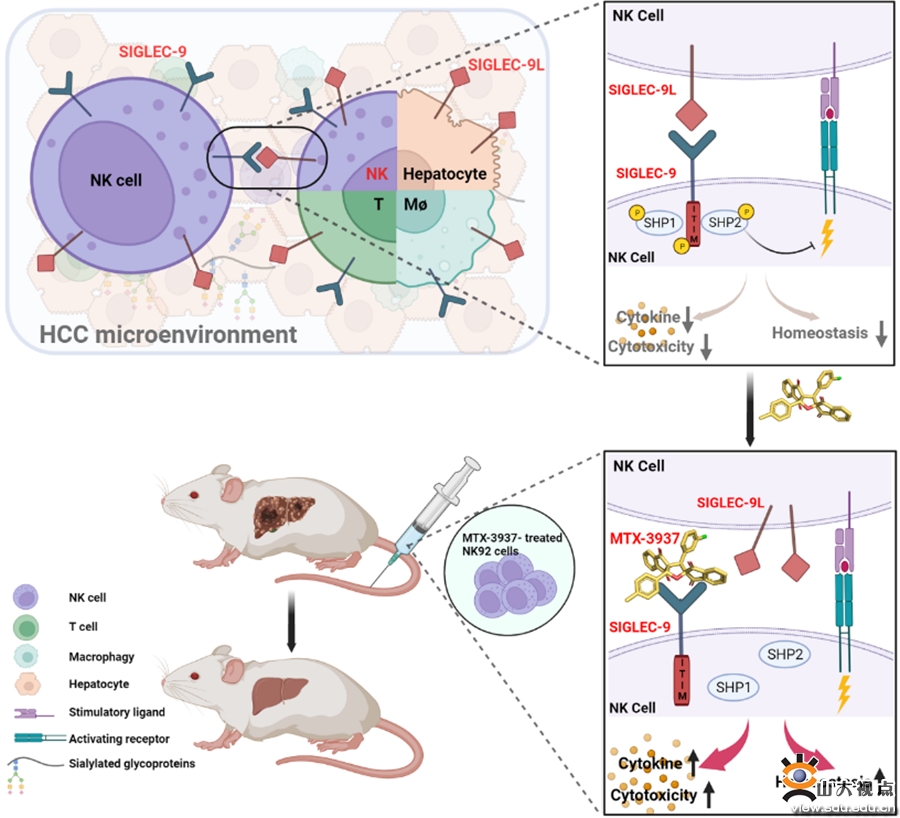
研究团队利用数据库分析和多标记免疫荧光对肝癌临床组织芯片中Siglec-7和Siglec-9与其配体的空间分布特征进行分析,发现Siglec-9及Siglec-9L显著高表达于TINK,且与预后负相关;进一步分析发现,在肿瘤组织中,与Siglec-9+ NK细胞与Siglec-9L+ NK细胞有更强的相互作用;而Siglec-7及其配体不参与调控肝癌发生发展。以上结果表明Siglec-9/Siglec-9L可作为NK细胞上肝癌免疫治疗的潜在干预靶点。接下来研究团队基于虚拟对接、生物膜干涉技术(BLI)和表面等离子共振技术(SPR),从306,709个小分子化合物中筛选到一个与Siglec-9结合的小分子化合物MTX-3937。体内外实验证实,MTX-3937通过抑制Siglec-9信号通路提高NK细胞抗肿瘤免疫,并抑制NK细胞的凋亡促进促进其稳态,表明MTX-3937可以作为先导化合物,具有HCC免疫治疗的临床应用前景。
综上,该研究阐明了HCC微环境中免疫细胞Siglec-9及其配体表达水平及预后相关性,阐明了HCC微环境中免疫细胞Siglec-9及其配体表达水平及预后相关性,筛选出具备肝癌治疗潜力的、靶向Siglec-9的小分子化合物MTX-3937,为肝癌免疫治疗提供了新的靶点和策略。
马春红教授团队长期致力于探索肿瘤免疫微环境调控机制及干预策略,相关研究成果发表在Gut, Nat Commun, Hepatology, J Hepatol, J Exp Med, Molecular Therapy, Cancer Res, Cell Mol Immunol, Cell Rep, Signal Transduct Target Ther, Adv Sci, J Immunother Cancer, Sci Transl Med等杂志。刘新泳教授团队长期致力于基于靶标结构和多种药物化学策略相结合的药物研究工作,聚焦于抗病毒药物、重大慢性病药物和免疫调节剂的先导发现、优化和药物开发。近年来已有多个抗病毒、抗痛风创新药物实现成果转化,相关成果在J Med Chem等期刊累计发表SCI论文400余篇。
【来源:山大视点 编辑:杨欣悦 审核:董慧敏】